Neue Designer-Proteine machen Isoforme nichtinvasiv sichtbar
Neue Designer-Proteine machen Isoforme nichtinvasiv sichtbar
Isoforme sind Varianten von Proteinen, die aus einem einzelnen Gen entstehen. Sie sind der Grund, warum wir weitaus mehr Proteine als Gene besitzen. Ein Ungleichgewicht der Isoforme steht in Verbindung mit vielen Krankheiten. Ein neues biotechnologisches Reportersystem mit Designer-Proteinen kann nun erstmals die Expression von Isoformen über längere Zeit hinweg in lebenden Zellen verfolgen. Das am Helmholtz Zentrum München und der Technischen Universität München entwickelte System hilft, regulatorische Mechanismen der Isoforme zu entschlüsseln und ermöglicht die Suche nach potenziellen Interventionszielen für molekulare Therapien.
Proteine sind die Hauptakteure unserer zellulären Prozesse und entstehen wie folgt: Zunächst kopiert die DNA einer Zelle ihre genetische Information auf die Boten-RNA (mRNA). Die Boten-RNA legt damit eine Sequenz von Aminosäuren fest. Die dabei entstehenden Aminosäureketten falten sich schließlich zu einem Protein zusammen. Tatsächlich führen aber unsere Gene nicht immer nur zu einer mRNA und einem Protein. Bei 90 Prozent unserer Gene erzeugt ein Prozess, der als alternatives Spleißen bezeichnet wird, mehrere mRNA-Varianten, von denen wiederum einige in einer bestimmten Zelle zu einem bestimmten Zeitpunkt in ein Isoform übersetzt werden. Bisherige Techniken, die alternatives Spleißen nachweisen können, sind meist arbeitsintensive Punktmessungen, die nicht zuverlässig über die Zeit hinweg verfolgen können, welche Isoforme in einer Zelle tatsächlich vorhanden sind.
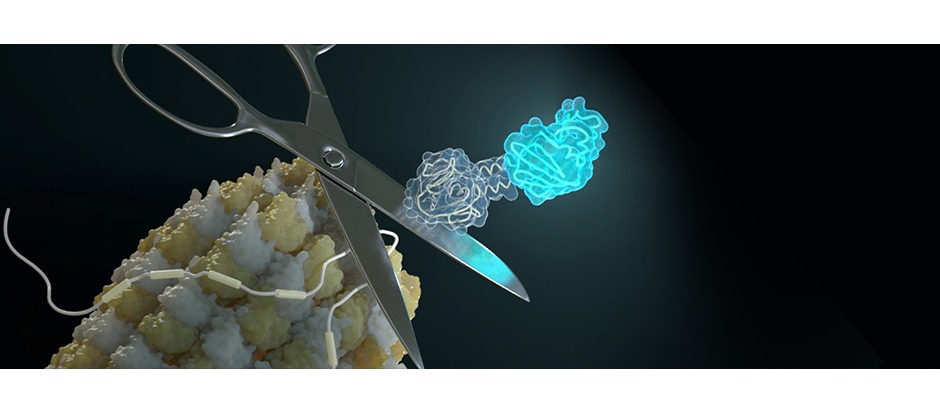
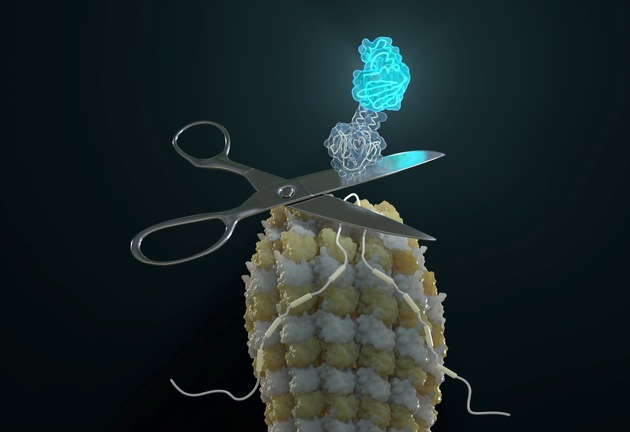
Forschende des Helmholtz Zentrums München und der Technischen Universität München (TUM) entwickelten daher ein neues biotechnologisches Reportersystem namens EXSISERS. Die Idee hinter EXSISERS ist es, ein Signal wie beispielsweise Licht zu erzeugen, sobald eine Isoform gebildet wird. „Möglich wird dies durch Designer-Proteine, die sich selbst aus der entstehenden Aminosäurekette herausschneiden können“, sagt Dong-Jiunn Jeffery Truong. „Sobald sie sich herausschneiden, leuchten sie auf und berichten damit über die Isoform-Bildung. Dabei hinterlässt das Designer-Protein keinerlei Spuren oder Narben am Isoform.“ Die Forschungsgruppe hat diese Methode bereits auf menschliche Zellen in Kultur angewandt. Dabei analysierten sie die Expression von Isoformen eines Proteins namens Tau, das mit neurodegenerativen Krankheiten wie Parkinson in Verbindung steht. Tau-Isoforme sind deshalb ein potenzielles Interventionsziel für molekulare Therapien.
„Inspiriert von natürlichen biomolekularen Prozessen werden wir mithilfe von Bioengineering künftig noch viele weitere grundlegende zelluläre Prozesse nichtinvasiv sichtbar machen können“, sagt Gil Gregor Westmeyer. „Je mehr Parameter wir in der Zelle überwachen können, desto besser können wir gezielte molekulare Therapien entwickeln, zum Beispiel zur Behandlung neurodegenerativer Erkrankungen.“ Westmeyer und seine Forschungsgruppe arbeiten bereits mit mehreren Laboren zusammen, die das neue Reportersystem nutzen, um ein umfassenderes Verständnis der Isoformexpression in Zellen und deren Auswirkungen auf Krankheiten zu erhalten.
Zu den Personen
Gil Gregor Westmeyer ist Direktor des Instituts für Synthetische Biomedizin am Helmholtz Zentrum München und Professor für Neurobiological Engineering an der TUM. Dong-Jiunn Jeffery Truong ist Gruppenleiter am Institut für Synthetische Biomedizin am Helmholtz Zentrum München und Erstautor dieser Studie.
Originalpublikation
Truong et al., 2021: Non-invasive and high-throughput interrogation of exon-specific isoform expression. Nature Cell Biology, DOI: 10.1038/s41556-021-00678-x
Helmholtz Zentrum München
Das Helmholtz Zentrum München verfolgt als Forschungszentrum die Mission, personalisierte medizinische Lösungen zur Prävention und Therapie umweltbedingter Krankheiten für eine gesündere Gesellschaft in einer sich schnell verändernden Welt zu entwickeln. Es erforscht das Entstehen von Volkskrankheiten im Kontext von Umweltfaktoren, Lebensstil und individueller genetischer Disposition. Besonderen Fokus legt das Zentrum auf die Erforschung des Diabetes mellitus, Allergien und chronischer Lungenerkrankungen. Der Hauptsitz des Zentrums liegt in Neuherberg im Norden Münchens. Das Helmholtz Zentrum München beschäftigt rund 2.500 Mitarbeitende und ist Mitglied der Helmholtz-Gemeinschaft, der größten Wissenschaftsorganisation Deutschlands mit mehr als 40.000 Mitarbeitenden in 19 Forschungszentren.
Helmholtz Zentrum München Deutsches Forschungszentrum für Gesundheit und Umwelt (GmbH) Ingolstädter Landstraße 1 D-85764 Neuherberg Telefon: +49 89 3187-0 Internet: www.helmholtz-muenchen.de E-Mail: presse@helmholtz-muenchen.de
Geschäftsführung: Prof. Dr. med. Dr. h.c. Matthias H. Tschöp, Kerstin Günther Registergericht: Amtsgericht München HRB 6466 Umsatzsteueridentifikationsnummer: DE 129521671 Aufsichtsratsvorsitzende: MinDir’in Prof. Dr. Veronika von Messling